Blog
Blog
Βιο-ομοειδή φάρμακα: Οι 8 προκλήσεις για την εισαγωγή τους στην αγορά

Μολονότι έχουν περάσει σχεδόν 20 χρόνια από τότε που εγκρίθηκε το πρώτο βιο-ομοειδές σκεύασμα στον κόσμο και συγκεκριμένα από την Ευρωπαϊκή Ενωση, οι προκλήσεις για την εισαγωγή τους στις αγορές παραμένουν.
Το πρώτο βιο-ομοειδές που εγκρίθηκε από τον EMA ήταν το Abseamed, το οποίο παρήχθη από τον κάτοχο της άδειας κυκλοφορίας MEDICE Arzneimittel Pütter GmbH & Co. KG. Ο FDA θέσπισε ένα πλαίσιο για τα βιο-ομοειδή, το οποίο εγκρίθηκε το 2009, όταν ψηφίστηκε ο νόμος για τον ανταγωνισμό στις τιμές και την καινοτομία των βιολογικών προϊόντων.
Σημειώνεται ότι τα περισσότερα βιο-ομοειδή φάρμακα έχουν εγκριθεί στους θεραπευτικούς τομείς της ανοσολογίας, των αιματολογικών και λεμφικών διαταραχών, της ογκολογίας και των ενδοκρινικών διαταραχών.
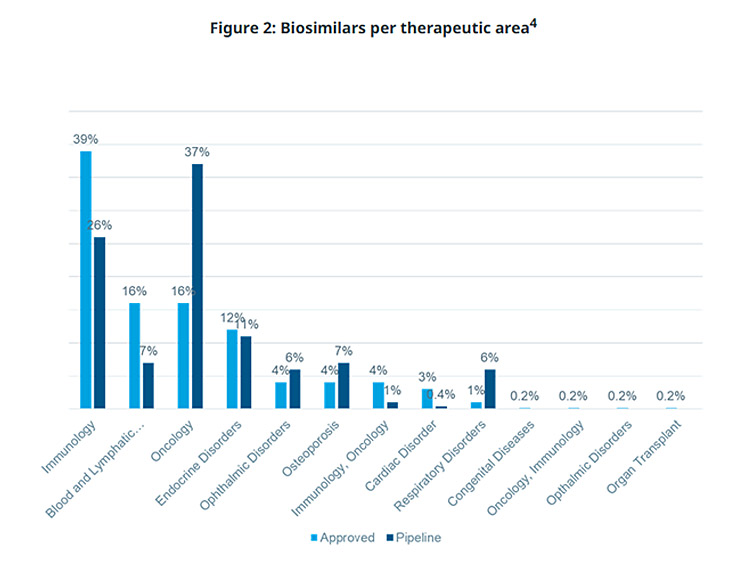
Προκλήσεις στις μελέτες βιο-ομοειδών
Τα βιο-ομοειδή έχουν γίνει μια υποσχόμενη λύση για τη μείωση του κόστους θεραπείας και την ενίσχυση της πρόσβασης των ασθενών σε βιολογικά φάρμακα που σώζουν ζωές. Παρ’ όλα αυτά, η εισαγωγή αυτών των σύνθετων μορίων στην αγορά είναι γεμάτη προκλήσεις, όπως:
- Προμήθεια προϊόντος αναφοράς: Επειδή το βιο-ομοειδές προϊόν βασίζεται στην επίδειξη της ομοιότητάς του με το προηγουμένως εγκεκριμένο προϊόν αναφοράς, είναι απαραίτητο να ληφθούν συγκεκριμένες παρτίδες του προϊόντος αναφοράς, να διασφαλιστεί η συνεχής προμήθειά του και να διαχειριστεί το κόστος για αυτό. Αναμένεται κάποια μεταβλητότητα μεταξύ των παρτίδων του φαρμάκου αναφοράς (π.χ., λόγω βιολογικής δραστηριότητας). Ωστόσο, μια τέτοια μεταβλητότητα θα μπορούσε να θέσει σε κίνδυνο την άσκηση συγκρισιμότητας, καθιστώντας βέλτιστη τη χρήση μόνο μίας παρτίδας στη φαρμακοκινητική- φαρμακοδυναμική ανάλυση (δηλαδή, μελέτη της κίνησης ενός φαρμάκου μέσω του σώματος και της βιολογικής απόκρισης του οργανισμού στο φάρμακο).
- Σχεδιασμός μελέτης: Για μελέτες βιοϊσοδυναμίας, συνιστάται ένας τυχαιοποιημένος, δύο περιόδων, δύο αλληλουχιών, διασταυρούμενος σχεδιασμός μίας δόσης. Για προϊόντα με μεγάλο χρόνο ημιζωής (ένα κοινό χαρακτηριστικό των βιο -ομοειδών προϊόντων), ένας σχεδιασμός διασταυρούμενης μελέτης θα οδηγούσε σε παρατεταμένες κλινικές μελέτες. Τέτοιες μακροχρόνιες μελέτες είναι επιρρεπείς σε υψηλά ποσοστά εγκατάλειψης των συμμετεχόντων και αυξημένη μεταβλητότητα των συμμετεχόντων, θέτοντας ενδεχομένως σε κίνδυνο την επιτυχή έκβαση της μελέτης.
- Τήρηση πρωτοκόλλου: Η εξοικείωση με το προϊόν αναφοράς ή/και την αγωγή του προϊόντος, καθώς και οι τοπικές πρακτικές, μπορούν να οδηγήσουν σε διακυμάνσεις στις διαδικασίες της μελέτης και αποκλίσεις από το πρωτόκολλο στα κέντρα μελέτης.
- Στρατολόγηση: Η στρατολόγηση ασθενών σε κλινικές δοκιμές ιστορικά αντιμετωπίζει δυσκολίες λόγω του ανταγωνισμού από άλλες δοκιμές, της προκατάληψης των ασθενών προς πειραματικές θεραπείες, της έλλειψης κινήτρων για τους ερευνητές και της έλλειψης πληροφοριών σχετικά με τις επερχόμενες δοκιμές. Εκτός από αυτά τα ευρέως αναγνωρισμένα εμπόδια, οι δοκιμές βιο-ομοειδών φαρμάκων αντιμετωπίζουν πρόσθετες προκλήσεις λόγω συγκεκριμένων κανονιστικών απαιτήσεων για την απόδειξη της ομοιότητας με το βιολογικό φάρμακο αναφοράς, όπως:
- Πρόσβαση σε καθιερωμένο πρότυπο περίθαλψης με αποδεδειγμένη αποτελεσματικότητα: Οι ασθενείς που ήδη λαμβάνουν θεραπεία με το SOC μπορεί να διστάζουν να στραφούν σε ένα βιο-ομοειδές λόγω φόβου μειωμένης αποτελεσματικότητας ή άγνωστων παρενεργειών. Οι ασθενείς που δεν έχουν λάβει προηγούμενη θεραπεία τείνουν επίσης να προτιμούν το SOC λόγω φόβου άγνωστης αποτελεσματικότητας/ παρενεργειών και λόγω της γνώσης τους για την αποδεδειγμένη αποτελεσματικότητα του SOC. Επιπλέον, οι γιατροί που δεν είναι ενημερωμένοι σχετικά με τα οφέλη ή το προφίλ ασφάλειας ενός βιο=ομοειδούς μπορεί να πιστεύουν ότι το SOC είναι ανώτερο και να διστάζουν να στρατολογήσουν ασθενείς για μια κλινική δοκιμή βιο-ομοειδούς. Η συνδυασμένη απροθυμία όλων των ενδιαφερόμενων μερών και η προτίμηση για το SOC μπορούν να επηρεάσουν σημαντικά την στρατολόγηση σε μια πειραματική κλινική δοκιμή βιο-ομοειδούς. Σε αυτήν την περίπτωση, η κατάλληλη επιλογή χώρας και τοποθεσίας παίζει κρίσιμο ρόλο.
- Αλλαγές στο πρότυπο περίθαλψης: Οι γιατροί, οι ασθενείς και οι επιτροπές δεοντολογίας μπορεί να διστάζουν να συμμετάσχουν σε μια κλινική δοκιμή βιο-ομοειδών εάν μια επερχόμενη πιθανή τυπική θεραπευτική αγωγή (SOC) αναμένεται να έχει καλύτερη αποτελεσματικότητα. Επιπλέον, οι ρυθμιστικοί φορείς ενδέχεται να απαιτήσουν τροποποιήσεις στον σχεδιασμό της δοκιμής ή να απαιτήσουν πρόσθετα δεδομένα για να διασφαλίσουν ότι το βιο-ομοειδές είναι συγκρίσιμο με τη νέα τυπική θεραπευτική αγωγή. Αυτό μπορεί να περιπλέξει τη δοκιμή, καθιστώντας την λιγότερο ελκυστική για τους ασθενείς και τους γιατρούς.
- Έλλειψη ενημέρωσης μεταξύ ερευνητών και ασθενών: Όταν οι γιατροί και οι ασθενείς δεν γνωρίζουν τις επερχόμενες δοκιμές στα βιο-ομοειδή, αυτό μπορεί να οδηγήσει σε ανεπαρκή στρατολόγηση. Ακόμα και αν οι πληροφορίες σχετικά με μια νέα δοκιμή διαδοθούν αποτελεσματικά, όλα τα ενδιαφερόμενα μέρη πρέπει να εκπαιδευτούν σχετικά με τη φύση και τα οφέλη ενός βιο-ομοειδούς.
- Ανταγωνισμός με κλινικές δοκιμές που διερευνούν νέα βιολογικά μόρια: Αρκετές δοκιμές που στοχεύουν την ίδια ένδειξη και ομάδα ασθενών καθιστούν δύσκολη την στρατολόγηση ασθενών για οποιαδήποτε κλινική δοκιμή. Όταν η πατέντα για προϊόντα αναφοράς πλησιάζει στη λήξη της, πολλές φαρμακευτικές εταιρείες στοχεύουν σε βιο-ομοειδή βιολογικά φάρμακα. Αυτό αυξάνει τον ανταγωνισμό για τις κλινικές δοκιμές βιο-ομοειδών. Οι περισσότεροι χορηγοί προτιμούν να στρατολογούν συμμετέχοντες από όλο τον κόσμο για να ολοκληρώσουν την εγγραφή πριν από άλλους χορηγούς. Τα νέα βιολογικά μόρια θεωρούνται πιο καινοτόμα με δυνατότητα καλύτερης αποτελεσματικότητας, καθιστώντας τα προτιμότερα έναντι των βιο-ομοειδών, των οποίων η αποτελεσματικότητα αναμένεται να είναι συγκρίσιμη με το αρχικό φάρμακο.
- Έλλειψη κινήτρων για ερευνητές και ασθενείς : Σε χώρες/τοποθεσίες όπου η τυπική περιγραφή του προϊόντος/βιολογικού παράγοντα αναφοράς είναι εύκολα προσβάσιμη, οι συγκριτικές μελέτες αποτελεσματικότητας και ασφάλειας για βιο-ομοειδή συχνά θεωρούνται από τους ερευνητές ως ελάχιστα επιστημονικού ενδιαφέροντος ή ως ελλιπείς ως προς τον καινοτόμο ή ενδιαφέροντα σχεδιασμό μελέτης. Οι ασθενείς μπορεί επίσης να μην βλέπουν κανένα πλεονέκτημα στη συμμετοχή τους σε μια μελέτη βιο-ομοειδών εάν έχουν πρόσβαση στο προϊόν αναφοράς ως μέρος της τυπικής φροντίδας τους.
Αντιμετώπιση προκλήσεων πρόσληψης σε συνεργασία με έμπειρους CRO
Για την επίτευξη φιλόδοξων στόχων προσέλκυσης ασθενών, οι χορηγοί θα πρέπει να δημιουργήσουν συνεργασίες με CRO που διαθέτουν εκτεταμένη εμπειρία, πρόσβαση σε κλινικά δεδομένα πραγματικού κόσμου, δίκτυα έμπειρων ερευνητών και πρόσβαση σε πλατφόρμες σύνδεσης ασθενών.
Για να διασφαλιστεί η έγκαιρη και επαρκής στρατολόγηση, είναι απαραίτητο οι χορηγοί να επικοινωνούν με τους ερευνητές, ώστε να κατανοούν την άποψή τους σχετικά με τα βιο- ομοειδή φάρμακα και να ευαισθητοποιουν το κοινό. Ο εντοπισμός των ανησυχιών των ερευνητών που θα μπορούσαν να επηρεάσουν το ενδιαφέρον τους για τη δοκιμή, η συζήτηση μαζί τους για την εξάλειψη της ανεπιθύμητης προκατάληψης προς τα βιο =ομοειδή και η τροποποίηση του σχεδιασμού/πρωτοκόλλου της δοκιμής πριν από τη μελέτη μπορούν να αποτρέψουν απροσδόκητες καθυστερήσεις στη στρατολόγηση.
Εκτός από τους ερευνητές, οι ασθενείς θα πρέπει να ενημερώνονται για το πώς τα βιο- ομοειδή μπορούν να προσφέρουν οικονομικά προσιτές εναλλακτικές λύσεις σε πιο ακριβές, επώνυμες βιολογικές θεραπείες, ενισχύοντας έτσι την πρόσβαση σε θεραπείες που διαφορετικά θα ήταν οικονομικά απρόσιτες.
Η επιλογή κατάλληλων χωρών και τοποθεσιών είναι κρίσιμη για τη διασφάλιση της βέλτιστης στρατολόγησης. Οι CRO μπορούν να παρέχουν στους χορηγούς ανάλυση βασισμένη σε δεδομένα, για να εντοπίσουν χώρες και αγορές με τις μεγαλύτερες ανεκπλήρωτες κλινικές ανάγκες.
Πηγές:
https://www.iqvia.com/blogs/2025/05/challenges-of-biosimilars-trials-and-how-cros-like-iqvia-can-help






